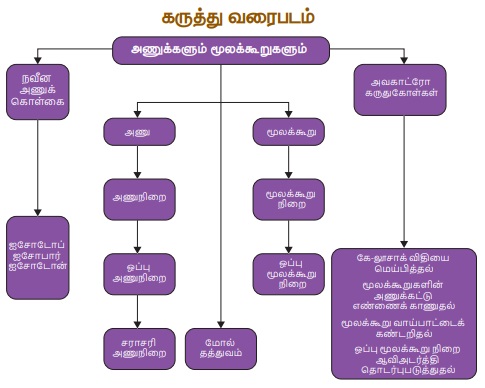
அணுக்களும் மூலக்கூறுகளும் | அறிவியல் - புத்தக வினாக்கள் விடைகள் | 10th Science : Chapter 7 : Atoms and Molecules
10வது அறிவியல் : அலகு 7 : அணுக்களும் மூலக்கூறுகளும்
புத்தக வினாக்கள் விடைகள்
அணுக்களும் மூலக்கூறுகளும் (அறிவியல்)
I. சரியான விடையைத் தேர்வு செய்க.
1. கீழ்கண்டவற்றுள் எது குறைந்த
நிறையைக் கொண்டது?
அ) 6.023 x 1023 ஹீலியம் அணுக்கள்
ஆ) 1 ஹீலியம் அணு
இ) 2 கி ஹீலியம்
ஈ) 1 மோல் ஹீலியம் அணு
2. கீழ்கண்டவற்றுள் எது மூவணு
மூலக்கூறு?
அ) குளுக்கோஸ்
ஆ) ஹீலியம்
இ) கார்பன் டை ஆக்ஸைடு
ஈ) ஹைட்ரஜன்
3. திட்ட வெப்ப அழுத்த நிலையில் 4.4 கி CO2 - ன்
பருமன்
அ) 22.4 லிட்டர்
ஆ) 2.24 லிட்டர்
இ) 0.24 லிட்டர்
ஈ) 0.1 லிட்டர்
4. 1 மோல் நைட்ரஜன் அணுவின் நிறை
அ) 28 amu
ஆ) 14 amu
இ) 28 கி
ஈ) 14 கி
5. 1 amu என்பது
அ) C - 12 ன் அணுநிறை
ஆ) ஹைட்ரஜன் அணுநிறை
இ) ஒரு C-12 அணுநிறையில் 1/12 பங்கின் முறை
ஈ) O – 16 ன் அணு நிறை
6. கீழ்கண்டவற்றுள் தவறான கூற்று
எது?
அ) ஒரு கிராம் C - 12 வானது அவகாட்ரோ எண்ணிக்கையிலான அணுக்களைக் கொண்டது.
ஆ) ஒரு மோல் ஆக்ஸிஜன் வாயுவானது அவகாட்ரோ
எண்ணிக்கையிலான மூலக்கூறுகளைக் கொண்டது.
இ) ஒரு மோல் ஹைட்ரஜன்
வாயுவானது அவகாட்ரோ எண்ணிக்கையிலான அணுக்களைக் கொண்டது.
ஈ) ஒரு மோல் எலக்ட்ரான் என்பது 6.023 × 1023
எலக்ட்ரான்களை குறிக்கிறது.
7. திட்ட வெப்ப அழுத்த நிலையில் 1 மோல் ஈரணு மூலக்கூறு வாயுவின் பருமன்
அ) 11.2 லிட்டர்
ஆ) 5.6 லிட்டர்
இ) 22.4 லிட்டர்
ஈ) 44.8 லிட்டர்
8. 20Ca40
தனிமத்தின் உட்கருவில்
அ) 20 புரோட்டான் 40 நியூட்ரான்
ஆ) 20 புரோட்டான் 20 நியூட்ரான்
இ) 20 புரோட்டான் 40 எலக்ட்ரான்
ஈ) 20 புரோட்டான் 20 எலக்ட்ரான்
9. ஆக்ஸிஜனின் கிராம் மூலக்கூறு
நிறை
அ) 16 கி
ஆ) 18 கி
இ) 32 கி
ஈ) 17 கி
10. 1 மோல்
எந்த ஒரு பொருளும் ................. மூலக்கூறுகளைக் கொண்டிருக்கும்.
அ) 6.023 × 1023
ஆ) 6.023 × 10-23
இ) 3.0115 × 1023
ஈ) 12.046 × 1023
II. கோடிட்ட இடங்களை நிரப்புக.
1. இரு வேறு தனிமங்களின்
அணுக்கள் ஒரே நிறை எண்ணையும் வேறுபட்ட அணு எண்ணையும் கொண்டிருந்தால் அவை ஐசோபார்கள்
எனப்படும்.
2. ஒரே நியூட்ரான்கள் எண்ணிக்கையை பெற்றுள்ள வெவ்வேறு தனிமங்களின்
அணுக்கள் ஐசோடோன்கள் எனப்படும்.
3. ஒரு தனிமத்தின் அணுக்களை
மற்றொரு தனிமத்தின் அணுக்களாகக செயற்கை மாற்று தனிமமாக்கல் முறையில் மாற்றலாம்.
4. புரோட்டான்கள் மற்றும்
நியூட்ரான்களின் கூடுதல் அந்த அணுவின் நிறை எண் எனப்படும்.
5. ஒப்பு அணுநிறை என்பது திட்ட அணு எடை எனவும் அழைக்கப்படுகிறது.
6. ஹைட்ரஜனின் சராசரி அணுநிறை 1.008 amu
7. ஒரு மூலக்கூறானது ஒரே
தனிமத்தின் அணுக்களால் உருவாக்கப்பட்டால் அவை ஒத்த அணு
மூலக்கூறு எனப்படும்.
8. ஒரு மூலக்கூறில் உள்ள
அணுக்களின் எண்ணிக்கையே அம்மூலக்கூறின் அணுக்கட்டு எண் ஆகும்.
9. திட்ட வெப்ப அழுத்த நிலையில் 22,400 மி.லி இடத்தை அடைத்துக் கொள்ளக் கூடிய வாயு 1 மோல் எனப்படும்.
10. பாஸ்பரஸின் அணுக்கட்டு எண் நான்கு
III. பொருத்துக:
1. 8 கி O2 - 4 மோல்கள்
2. 4 கி H2 - 0.25 மோல்கள்
3. 52 கி He - 2 மோல்கள்
4, 112 கி N2 – 0.5 மோல்கள்
5. 35.5 கி Cl2 - 13 மோல்கள்
விடை:
1. 8 கி O2 – 0.5 மோல்கள்
2. 4 கி H2 - 4 மோல்கள்
3. 52 கி He - 0.25 மோல்கள்
4, 112 கி N2 - 13 மோல்கள்
5. 35.5 கி Cl2 - 2 மோல்கள்
IV. சரியா தவறா? தவறு எனில்
கூற்றினை திருத்துக.
1. இரு தனிமங்கள் இணைந்து
ஒன்றுக்கு மேற்பட்ட சேர்மங்களை உருவாக்கும்.
விடை: சரி
2. மந்த வாயுக்கள் அனைத்தும்
ஈரணு மூலக்கூறுகள் ஆகும்.
விடை: தவறு
மந்தவாயுக்கள் அனைத்தும் ஓரணு மூலக்கூறுகள் ஆகும்.
3. தனிமங்களின் கிராம்
அணுநிறைக்கு அலகு இல்லை.
விடை: தவறு
தனிமங்களின் ஒப்பு அணுநிறைக்கு அலகு இல்லை.
4. 1 மோல்
தங்கம் மற்றும் 1 மோல் வெள்ளி ஆகியவை ஒரே எண்ணிக்கையிலான
அணுக்களைக் கொண்டிருக்கும்.
விடை: சரி
5. CO2 - ன் மோலார் நிறை 42கி
விடை: தவறு
CO2 - ன் மோலார் நிறை 44கி
V. பின்வரும் வினாக்களில் கூற்றும் அதனையடுத்து
காரணமும் கொடுக்கப்பட்டுள்ளன. பின்வருனவற்றுள் எது சரியான தெரிவோ அதனைத் தெரிவு
செய்க
அ) 'A' மற்றும் 'R' சரி R, A ஐ விளக்குகிறது.
ஆ) A சரி R தவறு
இ) A தவறு R சரி
ஈ) A மற்றும் R சரி R, A க்கான சரியான விளக்கம் அல்ல.
1. கூற்று (A): அலுமினியத்தின் அணுநிறை 27.
காரணம் (R): ஒரு அலுமினியம் அணுவின்
நிறையானது 1/12 பங்கு கார்பன் - 12 ன்
நிறையை விட 27 மடங்கு அதிகம்.
விடை: அ) A மற்றும் R சரி, R, A ஐ விளக்குகிறது.
2. கூற்று (A): குளோரின் ஒப்பு மூலக்கூறுநிறை 35.5 amu.
காரணம் (R): குளோரினின் ஐசோடோப்புகள்
இயற்கையில் சம அளவில் கிடைப்பதில்லை.
விடை: அ) A மற்றும் R சரி, R, A ஐ விளக்குகிறது.
VI. குறு வினாக்கள் :
1. ஒப்பு அணுநிறை - வரையறு.
ஒரு தனிமத்தின் ஒப்பு அணுநிறை என்பது
அத்தனிமத்தின் ஐசோடோப்புகளின் சராசரி அணு நிறைக்கும் C - 12
அணுவின் நிறையில் 1/12 பங்கின் நிறைக்கும் உள்ள விகிதமாகும்.
2. ஆக்ஸிஜனின் பல்வேறு
ஐசோடோப்புகளையும் அதன் சதவீத பரவலையும் குறிப்பிடுக.
• 8O16 - 99.757%,
• 8O17 - 0.038%
• 8O18 - 0.205%
3. அணுக்கட்டு எண் - வரையறு.
• ஒரு மூலக்கூறில் உள்ள அணுக்களின் எண்ணிக்கையே
அம்மூலக்கூறின் அணுக்கட்டு எண் ஆகும்.
• அணுக்கட்டுஎண் = மூலக்கூறு நிறை / அணு நிறை
4. வேறுபட்ட ஈரணு
மூலக்கூறுகளுக்கு 2 எடுத்துகாட்டு கொடு.
• வேறுபட்ட ஈரணு மூலக்கூறுகள் = HCl, CaO.
5. வாயுவின் மோலார் பருமன்
என்றால் என்ன?
• திட்டவெப்ப அழுத்த நிலையில் (S.T.P) ஒரு மோல் வாயுவானது 22.4 லிட்டர் அல்லது 22400 மி.லி பருமனை கொண்டிருக்கும்.
இது மோலார் பருமன் என அழைக்கப்படுகிறது.
• இது மோலார் பருமன் என அழைக்கப்படுகிறது.
6. அம்மோனியாவில் உள்ள
நைட்ரஜனின் சதவீத இயைபைக் கணக்கிடுக.
அம்மோனியாவின் (NH3) மூலக்கூறு நிறை = N × 1 + H × 3
= 14 × 1 + 1 × 3 = 14 + 3
அம்மோனியாவின் மூலக்கூறு நிறை = 17
அம்மோனியாவில் நைட்ரஜனின் சதவீத இயைபு =
அம்மோனியாவில் நைட்ரஜனின் நிறை / அம்மோனியாவின் மூலக்கூறு நிறை × 100
= 14 / 17 × 100 = 1400 / 17
அம்மோனியாவில் நைட்ரஜனின் சதவீத இயைபு = 82.35%.
VII. பொருந்தாததை எடுத்து எழுதி காரணம் கூறுக:
1. ஐசோடோப்பு, ஐசோதெர்மல், ஐசோபார், ஐசோடோன்
விடை: ஐசோதெர்மல்
காரணம் : மற்றவைகள் அணுக்கள், மூலக்கூறுகளின்
அணு, நிறை எண்களோடு தொடர்புடையது. ஐசோதெர்மல் என்பது
வெப்பநிலை மாறாமல் வினைபுரியச் செய்வது.
2. ஹீலியம், அலுமினியம், ஆர்கான், குளோரின்.
விடை: குளோரின்
காரணம் : மற்ற அனைத்தும் ஓரணு மூலக்கூறு, குளோரின்
ஈரணு மூலக்கூறு.
3. 18 கி H2O,
22.4 L CO2, 6.023 × 1023 இரும்பு அணு,
38 கி NaOH.
விடை: 38 கி NaOH
காரணம் : மற்றவைகள் அனைத்து ஒரு மோல் பொருள்கள், 1 மோல் NaOH ன் நிறை 40கி.
VIII. நெடு வினாக்கள்:
1. 0.18 கி நீர் துளியில் உள்ள
நீர் மூலக்கூறுகளின் எண்ணிக்கையை கணக்கிடுக.
விடை:
மோல்களின் எண்ணிக்கை = (கொடுக்கப்பட்ட) நிறை / மூலக்கூறு நிறை
= 0.18 / 18 = 0.01
கிராம் மூலக்கூறு நிறை H2O
= H × 2 + 0 × 1
= 1 × 2 + 16 × 1
= 2 + 16 = 18கி
மூலக்கூறுகளின் எண்ணிக்கை = மோல்களின் எண்ணிக்கை
× அவகாட்ரோ எண்
= 0.01 × 6.023 × 1023
= 6.023 × 1021
0.18 கி நீரிலுள்ள
மூலக்கூறுகளின் எண்ணிக்கை = 6.023 × 1023.
மாற்றுமுறை:
மோல்களின் எண்ணிக்கை = அவகாட்ரோ எண் × கொடுக்கப்பட்ட நிறை / கிராம் மூலக்கூறு நிறை
= 6.023 × 1023 × 0.18 / 18
= 6.023 × 1023 × 0.01
= 6.023 × 1021.
0.18கி நீரிலுள்ள மூலக்கூறுகளின்
எண்ணிக்கை 6.023 x 1023.
கிராம் மூலக்கூறு நிறை H2O
= H × 2 + 0 × 1
= 1 × 2 + 16 × 1
= 2 + 16 = 18கி
2. N2 + 3 H2 → 2 NH3 (N = 14; H= 1) 1 மோல் நைட்ரஜன்
= ------- கி + 3 மோல் ஹைட்ரஜன் = ----------
கி → 2 மோல் அம்மோனியா = --------- கி.
விடை:
ஒரு மோல் நைட்ரஜனின் நிறை N2 = 2 × N = 2 × 14 = 28 கி
3 மோல் ஹைட்ரஜனின் நிறை H2
= 3(2 × H) = 3 (2 × 1) = 6 கி
2 மோல் அம்மோனியாவின் நிறை NH3
= 2 [N × 1 + H × 3]
= 2 [14 × 1 + 1 × 3]
= 2 [14 + 3]
= 34 கி.
ஒரு மோல் நைட்ரஜன் = 28 கி + 3
மோல் ஹைட்ரஜன் = 6 கி =
2 மோல் அம்மோனியா 34 கி
3. மோல்களின் எண்ணிக்கையைக்
கண்டறிக.
அ) 27கி அலுமினியம்
ஆ) 1.51 × 1023 மூலக்கூறு NH4CI
விடை:
அ) 27கி
அலுமினியம்
அ) மோல்களின் எண்ணிக்கை = கொடுக்கப்பட்ட நிறை / அணு நிறை = 27 /
27 = 1
27கி அலுமினியத்தின் மோல்களின்
எண்ணிக்கை I.
ஆ) 1.51 × 1023 மூலக்கூறு NH4CI
மோல்களின் எண்ணிக்கை = மூலக்கூறுகளின்
எண்ணிக்கை / 6.023 × 1023
= 1.51 × 1023 / 6.023 × 1023 = 1.51 / 6.023 =
0.25
1.51 × 1023 மூலக்கூறுகளின்
மோல்களின் எண்ணிக்கை = 0.25.
4. நவீன அணுக்கொள்கையின்
கோட்பாடுகளை எழுதுக.
விடை:
* அணு என்பது பிளக்கக்கூடிய துகள் (எலக்ட்ரான், புரோட்டான்]
* ஒரு தனிமத்தின் அணுக்கள் வெவ்வேறு அணுநிறைகளைப் பெற்றுள்ளன. [ஐசோடோப்புகள்]
* வெவ்வேறு தனிமங்களின் அணுக்கள் ஒரே அணுநிறைகளைப் பெற்றுள்ளன (ஐசோபார்கள்)
* அணுவை ஆக்கவோ, அழிக்கவோ முடியாது. ஒரு தனிமத்தின் அணுக்களை மற்றொரு தனிமத்தின் அணுக்களாக
மாற்றமுடியும்.
* அணுவானது எளிய முழு எண்களின் விகிதத்தில் இருக்க வேண்டிய அவசியமில்லை.
(எ.கா குளுக்கோஸ் C6 H12 O6]
* அணு என்பது வேதிவினையில் ஈடுபடும் மிகச்சிறிய துகள்.
* ஒரு அணுவின் நிறையிலிருந்து அதன் ஆற்றலை கணக்கிட முடியும்,
5. ஒப்பு மூலக்கூறு நிறைக்கும்
ஆவி அடர்த்திக்கும் உள்ள தொடர்பை வருவி.
விடை:
ஒப்புமூலக்கூறு நிறை:
* ஒரு வாயு அல்லது ஆவியின் ஒப்பு மூலக்கூறு நிறை
என்பது ஒரு மூலக்கூறு வாயு அல்லது ஆவியின் நிறைக்கும் ஒரு ஹைட்ரஜன் அணுவின் நிறைக்கும்
இடையே உள்ள விகிதமாகும்.
ஆவி அடர்த்தி :
* மாறா வெப்ப மற்றும் அழுத்த நிலையில் ஒரு
குறிப்பிட்ட பருமனுள்ள வாயு அல்லது ஆவியின் நிறைக்கும் அதே பருமனுள்ள ஹைட்ரஜன்
அணுவின் நிறைக்கும் உள்ள விகிதமே ஆவி அடர்த்தி எனப்படும்.
ஆவி அடர்த்தி = தி.வெ.அ நிலையில் குறிப்பிட்ட பருமனுள்ள வாயு (அ) ஆவியின்
நிறை / அதே பருமனுள்ள ஹைட்ரஜன் அணுவின் நிறை
அவகாட்ரோ விதிப்படி சமபருமனுள்ள வாயுக்கள்
அனைத்தும் சம அளவு எண்ணிக்கையிலான மூலக்கூறுகளைக் கொண்டிருக்கும்.
ஒரு பருமனுள்ள வாயுவில் 'n' எண்ணிக்கையிலான மூலக்கூறுகள்
உள்ளதாக கொண்டால்
ஆவி அடர்த்தி (தி.வெ.அ) = 'n' மூலக்கூறு வாயு (அ) ஆவியின்
நிறை /
'n' மூலக்கூறு ஹைட்ரஜனின் நிறை
n = 1 எனக் கொண்டால்
ஆவி அடர்த்தி = 1 மூலக்கூறுவாயு (அ) ஆவியின் நிறை / 1
மூலக்கூறு ஹைட்ரஜனின் நிறை
ஹைட்ரஜன் ஈரணு மூலக்கூறு. எனவே
ஆவி அடர்த்தி = 1 மூலக்கூறுவாயு (அ) ஆவியின் நிறை / 2 ஹைட்ரஜன் அணுக்களின்
நிறை
ஆவி அடர்த்தி = 1 மூலக்கூறுவாயு (அ) ஆவியின் நிறை / 2 × 1 ஹைட்ரஜன் அணுவின் நிறை
ஆவி அடர்த்தி = ஒப்புமூலக்கூறு நிறை / 2
[ஒப்புமூலக்கூறு நிறை = 1 மூலக்கூறுவாயு (அ) ஆவியின் நிறை / 1 ஹைட்ரஜன்
அணுவின் நிறை]
2 × ஆவி அடர்த்தி = ஒப்பு
மூலக்கூறுநிறை.
IX. உயர் சிந்தனைக்கான வினாக்கள் : (HOTS)
1. கால்சியம் கார்பனேட்டை வெப்பப்படுத்தும்
போது கீழ்க்கண்டவாறு சிதைவடைகிறது.
CaCO3 → CaO
+ CO2
அ) இவ்வினையில் எத்தனை
மோல்கள் கால்சியம் கார்பனேட் ஈடுபடுகிறது?
ஆ) கால்சியம் கார்பனேட்டின்
கிராம் மூலக்கூறு நிறையைக் கணக்கிடு.
இ) இவ்வினையில் எத்தனை
மோல்கள் கார்பன் டை ஆக்சைடு வெளி வருகிறது?
விடை:
அ) இவ்வினையில் 1 மோல் கால்சியம் கார்பனேட் ஈடுபடுகிறது.
ஆ) கால்சியம் கார்பனேட்டின் கிராம் மூலக்கூறு
நிறை (CaCO3) = Ca × 1 + C × 1 + O × 3
= 40 × 1 + 12 × 1 + 16 × 3
= 40 + 12 + 48
= 100கி.
இ) 1 மோல் கார்பன் டை ஆக்சைடு இவ்வினையில் வெளிவருகிறது.
X. கணக்கீடுகள்:
1. கீழ்கண்டவற்றின் நிறையைக்
காண்க.
அ) 2 மோல்கள் ஹைட்ரஜன் மூலக்கூறு
ஆ) 3 மோல்கள் குளோரின் மூலக்கூறு
இ) 5 மோல்கள் சல்பர் மூலக்கூறு
ஈ) 4 மோல்கள் பாஸ்பரஸ் மூலக்கூறு
H2 ன் மூலக்கூறு நிறை
H2 = H × 2
= 1 × 2 = 2
விடை:
அ) 2 மோல்கள் ஹைட்ரஜன் மூலக்கூறு: நிறை = மோல்களின் எண்ணிக்கை ×
மூலக்கூறு நிறை
= 2 × 2
2 மோல்கள் ஹைட்ரஜனின் நிறை = 4கி
ஆ) 3 மோல்கள் குளோரின் மூலக்கூறு:
நிறை = மோல்களின் எண்ணிக்கை × மூலக்கூறு நிறை
= 3 × 71
3 மோல்கள் குளோரின்
மூலக்கூறின் நிறை = 213 கி.
குளோரின் மூலக்கூறு நிறை Cl2
Cl × 2 = 35.5 × 2 = 71
இ) 5 மோல்கள் சல்பர் மூலக்கூறு:
நிறை = மோல்களின் எண்ணிக்கை × மூலக்கூறு நிறை
5 மோல்கள் சல்பர்
மூலக்கூறின் நிறை = 5 × 256
= 1280 கி.
சல்பர் மூலக்கூறு நிறை S8
S × 8 = 32 × 8 = 256
ஈ) 4 மோல்கள் பாஸ்பரஸ் மூலக்கூறு:
நிறை = மோல்களின் எண்ணிக்கை × மூலக்கூறு நிறை
4 மோல்கள் பாஸ்பரஸ் மூலக்கூறின்
நிறை = 4 × 120
= 480 கி.
பாஸ்பரஸ் மூலக்கூறின் நிறை
P4 = P × 4 = 30 × 4 = 120
2. கால்சியம் கார்பனேட்டில் உள்ள
ஒவ்வொரு தனிமத்தின் சதவீத இயைபைக் காண்க.
[Ca = 40; C = 12; O = 16]
விடை:
மூலக்கூறு நிறை CaCO3 = Ca × 1 + C × 1 + 0 × 3
= 40 × 1 + 12 × 1 + 16 × 3
= 40 + 12 + 48 = 100 கி.
தனிமத்தின் நிறை சதவீதம் = சேர்மத்தில் உள்ள
ஒரு குறிப்பிட்ட தனிமத்தின் நிறை / சேர்மத்தின் மூலக்கூறு நிறை × 100
CaCO3 - ல்
கால்சியத்தின் நிறை சதவீதம் = 40 / 100 × 100 = 40%
CaCO3 - ல் கார்பனின்
நிறை சதவீதம் = 12/100 × 100 = 12%
CaCO3 - ல்
ஆக்ஸிஜன் நிறை சதவீதம் = 48/ 100 × 100 = 48%
3. Al2(SO4)3
உள்ள ஆக்ஸிஜனின் சதவீத இயைபைக் காண்க. [Al = 27; O = 16; S =
32]
விடை:
மூலக்கூறு AI2(SO4)3 = Al × 2 + 3 [S × 1 + O × 4]
= 27 × 2 + 3 [32 × 1 + 16 × 4]
= 54 + 3[32 + 64]
= 54 + 96 + 192 [ஆக்ஸிஜன்]
= 342 கி
தனிமத்தின் நிறை சதவீதம் = சேர்மத்தில் உள்ள
ஒரு குறிப்பிட்ட தனிமத்தின் நிறை / சேர்மத்தின் மூலக்கூறு நிறை × 100
AI2(SO4)3 ல் ஆக்சிஜன் மூலக்கூறுகளின் நிறை சதவீதம் 192 / 342 × 100 = 56.14%.
4. போரானின் சராசரி அணுநிறை 10.804
amu எனில் B-10 மற்றும் B-11 சதவீத பரவலைக் காண்க.
விடை:
இயற்கையில் கிடைக்கும் போரானில் B - 11, x% மற்றும் B - 10, (1 - x)% உள்ளது
எனக் கொள்வோம்.
சராசரி அணுநிறை = B - 10ன் நிறை + B – 11 ன் நிறை
10.804 = (1 - x) × 10 + x × 11
10.804 = 10 - 10 x + 11 x
10.804 = 10 + x
x = 10.804 – 10
x = 0.804.
எனவே இயற்கையில் கிடைக்கும் போரானில்
B - 11ன் சதவீதம் = 0.804
× 100 = 80.4%
இயற்கையில் கிடைக்கும் போரானில் B - 10 ன் சதவீதம் = (1 -
x) = (1 -0.804) × 100
= 0.196 × 100 = 19.6%
இயற்கையில் கிடைக்கும் போரானில் B - 11 80.4% சதவீதமும்,
B - 10 19.6% சதவீதமும் இருக்கிறது.